Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии
Зміст
Pезюме. Статья посвящена современным подходам к терапии сахарного диабета, осложненного поражением почек. Сахарный диабет является важнейшей проблемой современной медицины, что прежде всего обусловлено высокой распространенностью заболевания среди трудоспособного населения. Диабетическая нефропатия – одно из тяжелых хронических осложнений диабета, повышающее инвалидизацию и смертность пациентов. Диабетическая нефропатия является основной причиной развития терминальной почечной недостаточности в развитых странах и со временем затрагивает около 30% пациентов. Поражение почек у больных сахарным диабетом встречается в 6-7% случаев из общего числа нефропатий у пациентов, получающих лечение в специализированном нефрологическом отделении многопрофильного стационара. Первые проявления диабетической нефропатии развиваются через 3-4 года от дебюта заболевания и достигают своего пика через 15-20 лет. Понятие «хроническая болезнь почек» включает в себя поражение почек независимо от первичного диагноза, характеризующееся такими основными диагностическими критериями, как экскреция альбумина с мочой и значения скорости клубочковой фильтрации, которые являются маркерами повреждения почек. Методы предупреждения прогрессирования диабетической нефропатии включают в себя общие мероприятия по изменению образа жизни, контроль гликемии и артериального давления, коррекцию нарушений липидного обмена в сочетании с нефропротективной терапией. В настоящее время при выборе терапии у больных сахарным диабетом 2 типа в сочетании с хронической болезнью почек наряду с приемом метформина предпочтение отдается ингибиторам натрий-глюкозного котранспортера 2-го типа и агонистам рецепторов глюкагоноподобного пептида-1, обладающим нефропротективным эффектом.
В настоящее время сахарный диабет (СД) является одной из актуальных проблем современной медицины. Прежде всего это связано с высокой распространенностью заболевания среди трудоспособного населения. Согласно прогнозам, к 2040 г. число людей, страдающих СД в возрасте 20-79 лет, увеличится до 642 миллионов [1, 2].
Немаловажным является и социально-экономическое значение заболевания. Развитие хронических осложнений СД существенно увеличивает раннюю инвалидизацию и смертность больных [3].
Наибольшая опасность, безусловно, связана с развитием сердечно-сосудистых осложнений (ССО) у данных пациентов. Также важное место в этом ряду занимает и диабетическая нефропатия (ДН), которая развивается приблизительно у 20,1% и 6,3% больных СД 1 и 2 типа соответственно [4, 5].
Изучение проблемы поражения почек при СД имеет длительную историю. Еще в 1836 г. британский врач Ричард Брайт отметил наличие у больных СД протеинурии (ПУ), что является признаком почечного повреждения [6]. В дальнейшем в 1936 г. американскими патологоанатомами P. Kimmelstiel и C. Wilson впервые была описана патоморфология почек у пациентов, страдающих СД [7].
У больных СД 2 типа осложнения ДН занимают третье место среди причин смерти после сердечно-сосудистых заболеваний (ССЗ) и злокачественных новообразований [1]. Кроме того, на сегодняшний день нефропатия, ассоции-рованная с СД 2 типа, является главной причиной терминальной почечной недостаточности (ТПН) в Европе, США и Японии [8]. Ранняя диагностика и своевременное обеспечение лечебно-профилактических мероприятий больным СД являются залогом предупреждения развития ДН.
Определение, распространенность и патогенез ДН
Под ДН понимают специфическое поражение всех структур почек (клубочков, канальцев, интерстиция и сосудов), возникающее при СД и сопровождающееся формированием узелкового гломерулосклероза, что может приводить к развитию ТПН, требующей проведения заместительной почечной терапии (диализ, трансплантация). Повреждение клубочков связано с утолщением их базальной мембраны, увеличением объема мезангиального матрикса и последующим развитием узелкового и/или диффузного интеркапиллярного гломерусклероза. Тубулоинтерстициальные изменения заключаются в дистрофии и атрофии эпителия канальцев, фиброзе интерстиция, а сосудистые – в развитии артериогиалиноза и артериосклероза. «Специфическое поражение структур почек» означает, что при отсутствии гипергликемии структурные изменения почек, характерные для СД, не выявляются [9].
Распространенность ДН непрерывно увеличивается, что происходит в результате взаимодействия генетических и средовых факторов у больных как с 1, так и со 2 типом СД. По международным данным максимальный пик развития ДН наблюдается при длительности заболевания от 20 до 30 лет и составляет при СД 1 типа 30-40%, а при СД 2 типа – 35-50%. В России распространенность ДН в среднем составляет при СД 1 типа 19%, при СД 2 типа – 8%. В то же время активный скрининг больных СД 2 типа показывает, что истинная распространенность ДН превышает зарегистрированную от 2 до 8 раз [10, 11].
Частота выявления ДН находится в тесной зависимости от длительности СД. Эта зависимость более изучена при СД 1 типа вследствие более точного определения дебюта заболевания. Частота развития ДН у больных с длительностью СД 1 типа до 10 лет составляет 5–6%, до 20 лет – 20–25%, до 30 лет – 35–40%, до 40 лет – 45%, а максимальный пик развития ДН приходится на сроки от 15 до 20 лет существования СД. Важно отметить, что наряду с классическим диабетическим гломерулосклерозом у больных СД 2 типа часто развивается поражение почек недиабетического генеза (хронический пиелонефрит, мочекаменная болезнь, ишемическая нефропатия и т. д.). Возможность сочетания нескольких форм нефропатии значительно повышает риск необратимого ухудшения функции почек. Установлено, что у пациентов с впервые выявленным СД 2 типа микроальбуминурия (МАУ) уже обнаруживается в 15-40% случаев, ПУ – в 7-10%, а хроническая почечная недостаточность (ХПН) – в 1%. Скорее всего это отражает позднюю диагностику ДН вследствие низкой информированности врачей первичного звена. При относительно точном определении времени дебюта СД 2 типа прослеживается такая же, как и при СД 1 типа, зависимость частоты развития ДН от длительности заболевания: 7-10% при длительности СД 5 лет, 20-35% – при длительности 20-25 лет и 50-57% – при более длительных сроках течения болезни [11].
По данным ГВКГ им. Н. Н. Бурденко доля больных с ДН среди всех пациентов, получающих лечение в нефрологическом отделении, составляет в среднем 6,4% (рис. 1).
.png)
.gif)
В то же время обследование больных эндокринологического отделения ГВКГ им. Н. Н. Бурденко показало, что ДН диагностируется у 35,6% больных с СД 1 типа и 43,1% – СД 2 типа (рис. 2) при сроке заболевания 25 лет. Первые признаки ДН выявляются через 3-4 года от дебюта СД, и частота ее достигает максимума после 20 лет течения болезни.
ДН развивается под действием огромного ряда причин. Но из всего многообразия механизмов ее развития наиболее изученными и доказанными являются метаболические (гипергликемия, гиперлипидемия) и гемодинамические (внутриклубочковая гипертензия, артериальная гипертензия (АГ)).
Безусловно, одним из самых важных метаболических факторов, инициирующих повреждение почек, является гипергликемия. В условиях гипергликемии образуются стабильные продукты гликозилирования, которые приводят к нарушению конфигурации мембраны клубочков, пролиферации гладкомышечных клеток артериол и усилению перекисного окисления липидов. В конечном итоге происходит утолщение гломерулярной базальной мембраны и развитие гломерулосклероза. Кроме того, увеличивается экспрессия в подоцитах сосудистого эндотелиального фактора роста, который аутокринно усиливает свою активность и приводит к повреждению ткани почек [12].
Большую роль в развитии ДН играет гиперлипидемия. Окисленные липопротеиды низкой плотности, ростовые факторы и цитокины увеличивают синтез компонентов мезангиального матрикса, ускоряя склерозирование клубочков. В свою очередь липиды, профильтровавшиеся в первичную мочу, могут приводить к повреждению клеток почечных канальцев [13].
АГ у пациентов с СД является самым мощным фактором прогрессирования хронической болезни почек (ХБП), который во много раз превышает по своему влиянию гипергликемию и гиперлипидемию. Внутриклубочковая гипертензия является основным гемодинамическим фактором развития ДН, которая возникает вследствие токсического действия гипергликемии и активации вазодилатирующих гормонов с развитием дилатации приносящей клубочковой артериолы, с одной стороны, а с другой – за счет активации местного ангиотензина II с констрикцией выносящей почечной артериолы [14].
Классификация и клинические проявления ДН
Впервые детальная классификация стадий ДН была разработана датским исследователем С. Е. Mogensen в 1983 г. Основу ее составляли показатели функциональных и структурных изменений почек (изменения скорости клубочковой фильтрации (СКФ), утолщение базальных мембран клубочков, наличие МАУ или ПУ) [15].
До последнего времени в РФ использовалась классификация ДН от 2000 г., предусматривавшая следующие стадии: микроальбуминурии, ПУ с сохранной азотовыделительной функцией почек и ХПН [16].
Показатель креатинина сыворотки крови использовался долгое время как основной маркер нарушения азотовыделительной функции почек. Благодаря последним исследованиям стало ясно, что из-за компенсаторных возможностей почек его цифры долгие годы могут соответствовать нормальным значениям, в то время как СКФ уже снижена.
Современная классификация ДН основывается на принципах стадирования ХБП, которую возможно диагностировать, если в течение трех и более месяцев имеются отклонения в анатомо-морфологической структуре или функции почек вне зависимости от нозологического диагноза [9]. Уровень СКФ в настоящее время признан лучшим методом оценки функции почек в целом как у здоровых лиц, так и при различных заболеваниях. Именно ее уровень определяет различные стадии ХБП (табл. 1).
.gif)
.gif)
Оценка степени поражения почек у больных СД существенно изменилась. Произошел переход от изолированной оценки АУ/ПУ в качестве классического маркера ДН к определению стадии ДН в зависимости от уровня СКФ, дополняя ее индексацией АУ/ПУ. АУ/ПУ рассматриваются как маркеры патологии почек, которые отражают степень повреждения клубочкового аппарата почек (табл. 2).
По данным международных клинико-эпидемиологических исследований, ХБП регистрируется у 40-60% пациентов с СД 2 типа. По данным федерального регистра, в 2016 г. в среднем по РФ ХБП выявлялась у пациентов с СД 1 типа в 23% случаев и при СД 2 типа – в 6,9% случаев. СКФ менее 60 мл/мин у больных СД 1 типа с ДН встречается в 50-60% случаев при наличии стойкой ПУ и в 70–80% случаев – у пациентов с СД 2 типа [2].
По данным ГВКГ им. Н. Н. Бурденко, у 2/3 пациентов, получающих лечение в специализированном нефрологическом отделении с ДН, наиболее часто диагностируются ХБП на стадии 3-5 (табл. 3).
.gif)
У этих пациентов, кроме типичных осложнений СД, имеется высокий риск развития ССО. Кроме того, наличие ХБП высоких градаций вносит ряд ограничений в возможности сахароснижающей терапии.
У ДН отсутствуют специфические симптомы, клиническую картину определяют собственно проявления СД, его осложнения и проявления ХБП. Основными клиническими проявлениями ХБП являются АУ/ПУ, АГ, анемия, электролитные нарушения, ацидоз, нарушения фосфорно-кальциевого обмена, может присутствовать отечный синдром вследствие формирования нефротического синдрома и/или задержки жидкости в организме.
Диагностика ДН
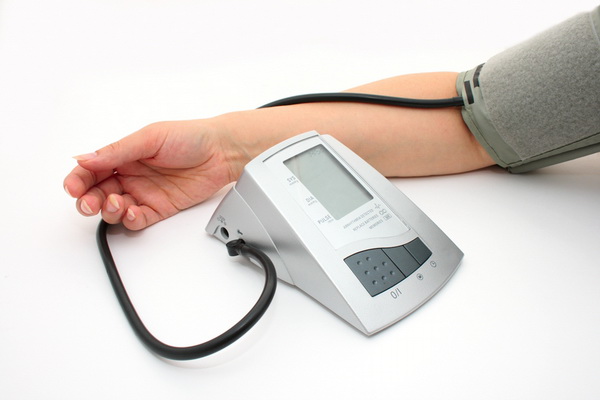
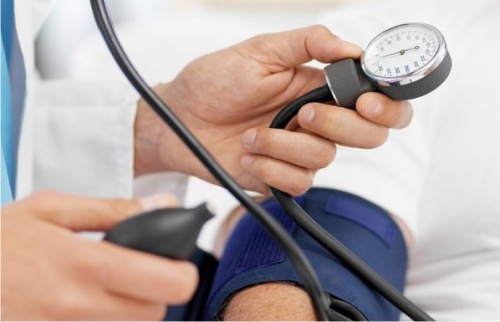
При появлении ПУ у больного СД с длительным анамнезом заболевания (более 10 лет), с выраженной диабетической ретинопатией и другими признаками микро- и макрососудистых осложнений диагноз ДН не вызывает сомнений. Для ее выявления выполняются обязательные методы лабораторной диагностики: определение соотношения альбумин/креатинин в утренней порции мочи, общеклинический анализ мочи с оценкой содержания белка, суточная ПУ, исследование осадка мочи, определение концентрации в сыворотке крови креатинина, мочевины и калия. При необходимости выполняются ультразвуковое исследование почек и сонографическое исследование почечных артерий.
В настоящее время в клинической практике для расчета СКФ у взрослого населения используют следующие расчетные формулы: Кокрофта–Голта 1976, MDRD 1999, CKD–EPI 2011.
Общепризнанным является тот факт, что наиболее точным расчетным методом определения СКФ является формула CKD–EPI [17].
СКФ = 141 × min(СКР/k, 1)a × max(СКР/k, 1) – 1,209 × 0,993возраст
[× 1,018 для женщин] [× 1,159 для лиц негроидной расы],
где СКР — креатинин сыворотки крови (мг/дл); k – 0,7 (для женщин) или 0,9 (для мужчин); a – коэффициент, равный – 0,329 (для женщин) или – 0,411 (для мужчин).
Поскольку в РФ величина креатинина измеряется в мкмоль/л, необходимо перевести ее в мг/дл, для этого значение нужно разделить на коэффициент 88,4 (т. е. 100 мкмоль/л соответствует 1,13 мг/дл).
Имеется ряд ситуаций, при которых расчетные методы применять не совсем корректно. К ним относятся:
- нестандартные размеры тела (пациенты с ампутированной конечностью, бодибилдеры);
- выраженное истощение и ожирение (индекс массы тела < 15 и > 40 кг/м2);
- беременность;
- заболевания скелетной мускулатуры (миодистрофия);
- параплегии и квадриплегии;
- вегетарианская диета;
- быстрое ухудшение функции почек (острый и быстропрогрессирующий нефритический синдромы);
- назначение нефротоксичных препаратов;
- решение вопроса о начале заместительной (диализной) почечной терапии;
- наличие почечного трансплантата.
В этих ситуациях СКФ необходимо определять с использованием клиренсовых методов (проба Реберга–Тареева).
Особенности сахароснижающей терапии при ДН
Принципы лечения ДН основаны на коррекции факторов прогрессирования ДН и ХБП с целью предупреждения развития ТПН и снижения риска ССО. Основными направлениями терапии являются компенсация нарушений углеводного, липидного, кальций-фосфорного обмена, анемии и достижение целевых значений АД.
Компенсация углеводного обмена играет ключевую роль в профилактике развития и замедлении прогрессирования ХБП у больных СД. Ряд клинических исследований показал, что строгий контроль гликемии позволяет не только предотвратить развитие ДН у лиц, не страдающих ею, но и затормозить прогрессирование этого осложнения у больных с АУ и ПУ. Это утверждение справедливо как для больных СД 1 типа (исследование DCCT), так и для больных СД 2 типа (исследование UKPDS) [11].
Прогрессирование азотемии, проявляющееся в снижении СКФ, значительно сужает спектр возможного применения пероральных сахароснижающих препаратов (табл. 4).
.gif)
Клинические практические рекомендациии KDIGO (Kidney Disease Improving Global Outcomes Quality Initiative – Инициатива по улучшению глобальных исходов заболеваний почек) рассматривают гликемический контроль как часть мультифакторной интервенционной стратегии, направленной на контроль АД и кардиоваскулярного риска. В них определены целевые уровни HbA1c у лиц с СД и ХБП с учетом имеющихся рисков. HbA1c < 7,0% (< 53 ммоль/моль) рекомендован для профилактики развития и прогрессирования микроваскулярных осложнений, включая ДН. У пациентов с риском гипогликемии не рекомендуется целевой уровень HbA1c < 7,0% (< 53 ммоль/моль). Для пациентов с выраженными осложнениями, сопутствующей патологией, небольшой ожидаемой продолжительностью жизни, риском гипогликемий целевое значение HbA1c < 8,0% [9, 17]. В последние десятилетия существенно изменились принципы назначения лекарственных препаратов, применяемых при лечении больных СД. В настоящее время основными требованиями к терапии является индивидуализированный, персонифицированный подход, обеспечивающий нефро- и ангиопротекцию, сердечно-сосудистую безопасность и строгий гликемический контроль [9].
Начало нынешнего века ознаменовались бурным ростом числа сахароснижающих препаратов (ССП) и появлением новых классов антидиабетических лекарственных средств с принципиально новыми механизмами действия: ингибиторы дипептилпептидазы-4 (иДПП-4), агонисты рецепторов глюкагоноподобного пептида-1 (арГПП-1), ингибиторы натрий-глюкозного котранспортера 2-го типа (НГЛТ-2). В завершенных крупномасштабных рандомизированных контролируемых исследованиях по оценке сердечно-сосудистых рисков этих препаратов были получены убедительные данные о том, что ингибиторы НГЛТ-2 снижают смертность от всех причин в большей степени, чем арГПП-1, в то время как иДПП-4 не продемонстрировали сердечно-сосудистых преимуществ в сравнении с плацебо и уступали ингибиторам НГЛТ-2 и арГПП-1 в отношении показателя смертности. Более того, полученные результаты исследований свидетельствуют о способности ингибиторов НГЛТ-2 улучшать сердечно-сосудистый прогноз и почечные исходы у пациентов с СД 2 типа. И ингибиторы НГЛТ-2, и арГПП-1 обладают выраженным сахароснижающим эффектом, способствуя значимому улучшению гликемического контроля, благоприятно влияют на массу тела и АД, а также не ассоциируются с повышенным риском гипогликемий. Оба класса препаратов проявляют кардио- и нефропротекторные свойства не только за счет прямого гипогликемического действия, но и благодаря многочисленным прямым и непрямым плейо-тропным метаболическим и гемодинамическим эффектам [19]. Необходимо отметить, что эти качества не являются класс-эффектом. Наиболее выраженными и доказанными кардио- и нефропротективными свойствами из ингибиторов НГЛТ-2 обладает препарат эмпаглифлозин.
Результаты исследования EMPA-REG OUTCOME показали, что прием эмпаглифлозина значительно сокращал начало или прогрессирование МАУ (снижение риска на 39% и 38% соответственно). В группе приема эмпаглифлозина отмечено снижение частоты случаев удвоения уровня сывороточного креатинина на 46%, частоты начала заместительной почечной терапии – на 55% по сравнению с плацебо. Последующее наблюдение пациентов продемонстрировало долгосрочную стабилизацию почечной функции в группе приема эмпаглифлозина. При этом сходный уровень СКФ не влиял на нефропротективные эффекты терапии эмпаглифлозином [20]. В исследовании CANVAS (влияние канаглифлозина на сердечно-сосудистые исходы) показано сокращение на 27% прогрессирования АУ при назначении препарата, а также замедление снижения СКФ и уменьшение случаев смерти от почечных причин на 40% [21].
Прием препарата группы арГПП-1 лираглутида в исследовании LEADER приводил к статистически значимому снижению комбинированного показателя частоты развития микрососудистых осложнений (отношение риска – ОР 0,84 при 95% ДИ от 0,73 до 0,97; p = 0,02). Причем такое снижение в основном было обусловлено более низкой частотой развития нефропатии в группе лираглутида по сравнению с группой плацебо (1,5 и 1,9 случая на 100 человеко-лет наблюдения соответственно; ОР 0,78 при 95% ДИ от 0,67 до 0,92; p = 0,003). В исследовании SUSTAIN-6 у пациентов, получавших семаглутид, так же, как и в LEADER, был более низкий риск возникновения или прогрессирования нефропатии преимущественно за счет снижения АУ, но более высокий риск осложнений диабетической ретинопатии, чем у пациентов в группе плацебо [22].
По результатам исследований иДДП-4 показали свою безопасность в отношении ССЗ, а при оценке функции почек наблюдалось снижение АУ в течение 3–6 месяцев, тогда как СКФ оставалась стабильной в течение всего периода наблюдения [22].
Результаты проведенных исследований привели к пересмотру рекомендаций по лечению СД 2 типа и профилактике ССЗ у этой категории больных. В настоящее время как в международных, так и в отечественных клинических рекомендациях предлагается при выборе терапии у отдельных категорий больных СД 2 типа с ССЗ, ХБП наряду с метформином отдавать предпочтение арГПП-1 и ингибиторам НГЛТ-2 [9]. Важным отличием обновленных клинических рекомендаций является фокус на раннее применение ингибиторов НГЛТ-2 или арГПП-1 при лечении СД 2 типа с целью предупреждения неблагоприятных сердечно-сосудистых и почечных исходов независимо от достижения гликемического контроля при терапии метформином.
Заключение
Таким образом, поражение почек при СД встречается у 6-7% пациентов, получающих лечение в специализированном нефрологическом отделении многопрофильного стационара, однако в основном это больные с ХБП 3-5 стадии, имеющие высокие риски ССО и прогрессирования почечной недостаточности. Первые проявления ДН развиваются через 3-4 года от дебюта заболевания и достигают своего максимума через 15-20 лет. Ранняя диагностика ДН, основанная на выявлении и оценке выраженности альбуминурии и/или ПУ и динамики СКФ, является залогом эффективного лечения. Важнейшим звеном терапии больных с ДН является назначение сахароснижающих препаратов с доказанным нефропротективным эффектом.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
- World Health Organization 2019. URL: https://www.who.int/diabetes/global-report/en/.
- Дедов И. И., Шестакова М. В., Викулова О. К., Исаков М. А., Железнякова А. В. Атлас регистра сахарного диабета Российской Федерации. Статус 2018 года // Сахарный диабет. 2019; 2S (22): 4-61. [Dedov I. I., Shestakova M. V., Vikulova O. K., Isakov M. A., Zheleznyakova A. V. Atlas of the diabetes register of the Russian Federation. Status of 2018 // Sakharnyy diabet. 2019; 2S (22): 4-61.]
- Bommer C., Heesemann E., Sagalova V., Manne-Goehler J., Atun R., Bärnighausen T. et al. The global economic burden of diabetes in adults aged 20-79 years: a cost-of-illness study // Lancet Diabetes Endocrinol. 2017; 5: 423-430. URL: https://doi.org/10.1016/S2213-8587(17)30097-9.
- Global Burden of Metabolic Risk Factors for Chronic Diseases Collaboration. Cardiovascular disease, chronic kidney disease, and diabetes mortality burden of cardiometabolic risk factors from 1980 to 2010: a comparative risk assessment // Lancet Diabetes Endocrinol. 2014; 2: 634-647.
- Шестакова М. В., Кошель Л. В., Вагодин В. А., Дедов И. И. Факторы риска прогрессирования диабетической нефропатии у больных с длительным течением сахарного диабета, по данным ретроспективного анализа // Тер. арх. 2006; 5: 26-28. [Shestakova M. V., Koshel’ L. V., Vagodin V. A., Dedov I. I. Risk factors for the progression of diabetic nephropathy in patients with long-term diabetes mellitus, according to a retrospective analysis // Ter. arkh. 2006; 5: 26-28.]
- Rabcin R., Fervenza F. C. Renal Hypertrophy and Kidney Disease in Diabetes // Diabetes Metab Rev. 1996; 12: 217-241.
- Kimmelstiel P., Wilson C. Intercapillary lesion in the glomeruli of the kidney // Am. J. Pathol. 1936; 12: 82-97.
- Remuzzi G., Schieppati A., Ruggenenti P. Clinical practice. Nephropathy in Patients with Type 2 Diabetes // N. Engl. J. Med. 2002; 346 (15): 1145-1151.
- Алгоритмы специализированной медицинской помощи больным сахарным диабетом: клин. рек. / Под ред. И. И. Дедова, М. В. Шестаковой, А. Ю. Майорова // Сахарный диабет. 9-й вып. М.: 2019. 212 с. [Algorithms of specialized medical care for patients with diabetes mellitus: wedge. rivers. / Pod red. I. I. Dedova, M. V. Shestakovoy, A. Yu. Mayorova // Sakharnyy diabet. 9-y vyp. M.: 2019. P. 212.]
- Fioretto P., Caramori M. L., Mauer M. The kidney in diabetes: dynamic pathways of injury and repair. The Camillo Golgi lecture 2007 // Diabetologia. 2008; 51: 1347-1355.
- Шестакова М. В., Шамхалова М. Ш., Ярек-Мартынова И. Я. и др. Сахарный диабет и хроническая болезнь почек: достижения, нерешенные проблемы и перспективы лечения // Сахарный диабет. 2011; 1: 81-88. [Shestakova M. V., Shamkhalova M. Sh., Yarek-Martynova I. Ya. i dr. Diabetes Mellitus and Chronic Kidney Disease: Achievements, Unresolved Issues and Treatment Prospects // Sakharnyy diabet. 2011; 1: 81-88.]
- Бобкова И. Н., Шестакова М. В., Щукина А. А. Диабетическая нефропатия – фокус на повреждение подоцитов // Нефрология. 2015; 19 (2): 33-43. [Bobkova I. N., Shestakova M. V., Shchukina A. A. Diabetic nephropathy – focus on podocyte damage // Nefrologiya. 2015; 19 (2): 33-43.]
- Захарьина О. А., Тарасов А. А., Бабаева А. Р. Актуальные аспекты медикаментозной профилактики и лечения диабетической ангиопатии // Лекарственный вестник. 2012; 5 (45): 14-22. [Zakhar’ina O. A., Tarasov A. A., Babayeva A. R. Actual aspects of drug prevention and treatment of diabetic angiopathy // Lekarstvennyy vestnik. 2012; 5 (45): 14-22.]
- Шестакова М. В. Роль тканевой ренин-ангиотензин-альдостероновой системы в развитии метаболического синдрома, сахарного диабета и его сосудистых осложнений // Сахарный диабет. 2010; 3: 14-19. [Shestakova M. V. The role of the tissue renin-angiotensin-aldosterone system in the development of metabolic syndrome, diabetes mellitus and its vascular complications // Sakharnyy diabet. 2010; 3: 14-19.]
- Mogensen C. E., Christensen C. K., Vittinghus E. The stages in diabetic renal disease. With emphasis on the stage of incipient diabetic nephropathy // Diabetes. 1983; 32 (2): 64-78.
- Шестакова М. В. Диабетическая нефропатия: фатальное или предотвратимое осложнение? // Рус. мед. журнал. http://www.rmj.ru/2007/3. [Shestakova M. V. Diabetic nephropathy: a fatal or preventable complication? // Rus. med. zhurnal. http://www.rmj.ru/2007/3.]
- Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury // Kidney Int Suppl. 2012; Issue 1: 1-126.
- Lim S., Eckel R. H., Koh K. K. Clinical implications of current cardiovascular outcome trials with sodium glucose cotransporter-2 (SGLT2) inhibitors // Atherosclerosis. 2018; 272: 33-40.
- Handelsman Y. Rationale for the early use of sodium-glucose cotransporter-2 inhibitors in patients with type 2 diabetes // Advances in Therapy. 2019; 36 (10): 2567-2586.
- Wanner C., Inzucchi S. et al. Empaglifozin and progression of kidney disease in type 2 diabetes // N. Engl J. Med. 2016; 375: 323–334.
- Jakher H., Chang T. I., Tan M., Mahaffey K. W. Canagliflozin review – safety and efficacy profile in patients with T2DM // Diabetes Metab. Syndr. Obes. 2019; 12: 209-15. DOI: 10.2147/DMSO.S184437.
- Prischl F. C., Wanner C. Renal Outcomes of Antidiabetic Treatment Options for Type 2 Diabetes-A Proposed MARE Definition // Kidney Int. Rep. 2018; 3 (5): 1030-8. DOI: 10.1016/j.ekir.2018.04.008.
А. Г. Борисов*, **, 1, кандидат медицинских наук
С. В. Чернавский*, **, доктор медицинских наук
М. А. Смирнова**, кандидат медицинских наук
А. А. Стремоухов**, доктор медицинских наук, профессор
* ФГБУ ГВКГ им. Н. Н. Бурденко МО России, Москва, Россия
** ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
1Контактная информация: bag22@rambler.ru
Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии/ А. Г. Борисов, С. В. Чернавский, М. А. Смирнова, А. А. Стремоухов
Для цитирования: Борисов А. Г., Чернавский С. В., Смирнова М. А., Стремоухов А. А. Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии // Лечащий Врач. 2021; 9 (24): 53-58. DOI: 10.51793/OS.2021.24.9.010
Теги: сахарный диабет, почки, контроль гликемии, нефропротективная терапия
Купить номер с этой статьей в pdf
Подписывайтесь на нашу email рассылку и оставайтесь в курсе самых важных медицинских событий
- Ученые: кожу человека можно заставить регенерировать
- Место азитромицина в комплексной терапии COVID-19. Преимущества и эффективность применения диспергируемой формы в амбулаторных условиях
- Исследование опровергло связь гормонозаместительной терапии и деменции
- Современные возможности терапии больных атопическим дерматитом ингибиторами Янус-киназы
- Обида на родителей
- 7 тыс. шагов в день — это новые 10 тыс. шагов